
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
Volgens de wet van Coulomb, als de atomair aantal neemt toe binnen een reeks van atomen , de nucleaire aantrekkingskracht want elektronen zullen ook toenemen, waardoor de elektronen dichter bij de kern worden getrokken. Zo'n relatie tussen atomair nummer en atomaire straal is een directe correlatie.
Evenzo, wat is de relatie tussen atoomnummer en atoomstraal?
De atoomnummer is de hoeveelheid protonen aanwezig in de atoom . Daarom kunnen we zeggen dat de atoomnummer vertegenwoordigt de positieve lading van de atoom . Als de positieve lading van de atoom verhoogt de atomaire straal neemt af omdat de positieve lading elektronen dichter bij de kern zal brengen.
Men kan zich ook afvragen, wat is coulombkracht en hoe wordt deze beïnvloed door kernlading? de effectieve nucleaire lading van een atoom is de netto positieve opladen 'gevoeld' door het VALENCE-elektron. Dit betekent rekening houden met de aantrekkelijke krachten gevoeld tussen de protonen en elektronen evenals de replusive krachten gevoeld tussen de valentie-elektronen en de kern (binnenste) elektronen.
Dit in overweging nemend, waar hangt de coulomb-aantrekking van af?
Dit coulomb attractie zorgt ervoor dat elektronen rond de kern draaien.) De sterkte van de coulomb aantrekkingskracht hangt af van twee dingen: de grootte van het atoom. De totale lading van het atoom.
Wat is de relatie tussen coulomb aantrekking en ionisatie-energie?
Hoe groter de ionisatieenergie , hoe moeilijker het is tot een elektron verwijderen. Hetzelfde gebruiken Coulomb attractie ideeën, we kunnen de eerste uitleggen ionisatieenergie trends op het periodiek systeem. De tendens van een atoom in een molecuul tot trekken gedeelde elektronen aan tot zelf heet elektronegativiteit.
Aanbevolen:
Hoe verhoudt het woord matrix zich tot mitochondriën?
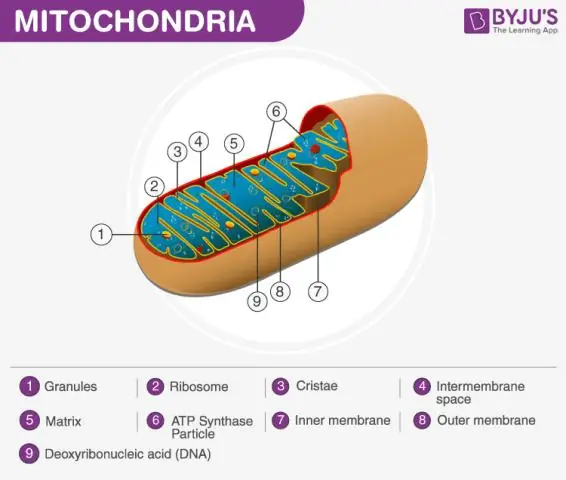
De mitochondriale matrix gedefinieerd Het mitochondrion bestaat uit een buitenmembraan, een binnenmembraan en een gelachtig materiaal dat de matrix wordt genoemd. Deze matrix is stroperiger dan het cytoplasma van de cel omdat het minder water bevat. Dit is een belangrijke stap in de cellulaire ademhaling, die energiemoleculen produceert die ATP . worden genoemd
Hoe verhoudt uw antwoord uit vraag 1 zich tot het Linnaeaanse classificatiesysteem?

Hoe verhoudt uw antwoord uit vraag 1 zich tot het Linnaeaanse classificatiesysteem? Mijn antwoord op vraag 1 heeft betrekking op het Linnaen Classificatiesysteem door eerst de binnen- en buitenkant van het organisme te identificeren. Daarna gebruikt de Linneaanse classificatie kleur en grootte om het organisme te identificeren
Hoe verhoudt de Oost-Afrikaanse Rift zich tot platentektoniek?

De East African Rift Valley (EAR) is een zich ontwikkelende divergerende plaatgrens in Oost-Afrika. De Nubische en Somalische platen scheiden zich ook van de Arabische plaat in het noorden, waardoor een 'Y'-vormig scheursysteem ontstaat. Deze platen kruisen elkaar in de Afar-regio van Ethiopië op wat bekend staat als een 'triple junction'
Hoe verhoudt de kinetische theorie van materie zich tot vaste stoffen, vloeistoffen en gassen?

De kinetische moleculaire theorie van materie stelt dat: Materie bestaat uit deeltjes die constant in beweging zijn. Alle deeltjes hebben energie, maar de energie varieert afhankelijk van de temperatuur waarin het monster zich bevindt. Dit bepaalt op zijn beurt of de stof in vaste, vloeibare of gasvormige toestand bestaat
Hoe verhoudt de wet van Coulomb zich tot ionisatie-energie?

De ionisatie-energie van een atoom is het energieverschil tussen het in het atoom gebonden elektron en het elektron op oneindige afstand van het atoom. De wet van Coulomb geeft de elektrische potentiële energie tussen twee puntladingen met de afstand r ertussen. De energie is omgekeerd evenredig met deze afstand
