
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-06-01 05:05.
Basiciteit. In vergelijking met aminen, amiden zijn zeer zwakke basen. Terwijl het geconjugeerde zuur van een amine een pKa heefteen van ongeveer 9,5, het geconjugeerde zuur van an amide heeft een pKeen rond − 0,5. Daarom, amiden hebben niet zo duidelijk waarneembare zuur-base-eigenschappen in water.
Ook gevraagd, wat is de pKa van een amine?
De waarde van 10,63 verwijst eigenlijk naar de pKa van het geconjugeerde zuur van methyl amine , NIET methylamine zelf. Het is een pKaH-waarde. Evenzo vermeldt dezelfde tabel trimethylamine met a pKa van 9.8.
Kunnen amiden ook worden geprotoneerd? EEN geprotoneerde amide bezit de minst zure groep van allemaal (CONH+), het bewijs dat de knipperende resonantievorm in dit geval een overweldigende bijdrage levert. Het eenzame elektronenpaar op NH2 is zeer gedelokaliseerd naar de carbonylgroep in amiden . Eigenlijk de C=O. groep van een amide is fundamenteler dan de NH2.
Evenzo kun je je afvragen, wat is de pKa van hydroxide?
Hydroxide ion, HO(-) staat niet aan de linkerkant van de pKa tabel, maar het is op de "inverse" pKa tafel - het is de geconjugeerde basis van water, H2O. Water heeft een pKa van ~15, en CH4 heeft een pKa van 50. Ons product is een sterker zuur. Van het omgekeerde pKa tabel, merken we ook op dat CH3(-) is een sterkere basis dan HO(-).
Waarom zijn amiden basisch?
In tegenstelling tot aminen, die behoorlijke basen zijn, amiden zijn zwakke basen. De geconjugeerde zuren van amiden hebben pKa-waarden van ongeveer -0,5. De reden amiden zijn niet zo basis komt door de aanwezigheid van de carbonylgroepen. amiden kunnen ook waterstofbruggen omdat ze een N-H-binding bevatten.
Aanbevolen:
Waarom werkt een buffer het beste bij een pH in de buurt van zijn pKa?
Met andere woorden, de pH van de equimolaire oplossing van zuur (bijvoorbeeld wanneer de verhouding van de concentratie van zuur en geconjugeerde base 1:1) is, is gelijk aan de pKa. Dit gebied is het meest effectief om weerstand te bieden aan grote veranderingen in pH wanneer zuur of base wordt toegevoegd. Een titratiecurve toont visueel de buffercapaciteit aan
Wat is een amide in de chemie?

Een amide is een functionele groep die een acarbonylgroep bevat die is gekoppeld aan een stikstofatoom of een verbinding die de functionele amidegroep bevat. Amiden zijn afgeleid van carbonzuur en een amine. Amide is ook de naam voor het anorganische anion NH2
Wat is de eerste stap bij het construeren van een loodlijn van een punt op een lijn?
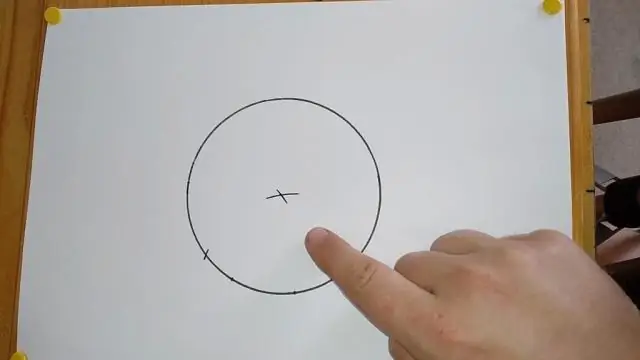
Verbind het gegeven punt met het punt waar de bogen elkaar kruisen. Gebruik een liniaal om ervoor te zorgen dat de lijn recht is. De lijn die je tekent staat loodrecht op de eerste lijn, door het gegeven punt op de lijn
Wat is een voorbeeld van een gedeelde afgeleide eigenschap van een primaat?

Apomorfie - een afgeleide eigenschap die niet wordt gevonden in de voorouder, maar wel aanwezig is in afstammelingen, bijvoorbeeld nagels bij primaten. Autapomorphy - een unieke afgeleide eigenschap die aanwezig is in lidsoorten van een bepaalde graad, bijvoorbeeld het ontbreken van een staart bij apen
Wat is de flux door een kubus van zijde als een puntlading van Q zich in een van zijn hoeken bevindt?

Zoals we dat weten, is de totale flux van een lading q q/ε0 (wet van Gauss). Als de lading zich op de hoek van een kubus bevindt, komt een deel van de flux de kubus binnen en verlaat deze via enkele van zijn vlakken. Maar een deel van de flux komt niet in de kubus. Deze 1/8e wordt weer opgedeeld in 3 delen
