
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
Hoe verschilt water onder het smeltpunt en daarboven? het? Onderstaand het blijft dicht bij elkaar en ze stuiteren van elkaar af. Bovenstaand de moleculen komen zelfs dichterbij dan onderstaand . De kokend /condensatie punt van water bedraagt 373K.
Waarom zijn de smelt- en vriespunten hetzelfde?
Bevriezen en smeltend zijn gewoon verschillende termen die worden gebruikt om de overgang tussen de vaste en vloeibare toestand van een materiaal te beschrijven. Bevriezen betekent meestal dat er energie wordt verwijderd uit een materiaal (vloeibaar verandert in vast) en smeltend betekent meestal dat er energie aan een materiaal wordt toegevoegd (vaste stof verandert in vloeistof).
Men kan zich ook afvragen, verlaagt water het smeltpunt? Smeltend neemt warmte op ("latente warmte") omdat de vloeistof meer energie heeft dan de vaste stof. Dat koelt het ijs en het zoute water tot minder dan 0°C. Dus ja, het doet lager de werkelijke temperatuur.
Evenzo kunt u zich afvragen: hoe weet u of het smeltpunt van een verbinding boven of onder kamertemperatuur ligt?
Indien de normaal smeltpunt van een stof is onder kamertemperatuur , de substantie is een vloeistof bij kamertemperatuur . benzeen smelt bij 6°C en kookt bij 80°C; het is een vloeistof bij kamertemperatuur . Indien beide normaal smeltpunt en de normaal kookpunt zijn boven kamertemperatuur , de substantie is een vaste stof.
Welke stof heeft een hoger smeltpunt dan water?
Natriumchloride smelt bij 801°C. IJs (vast H 2 O) is een moleculaire verbinding waarvan de moleculen bij elkaar worden gehouden door waterstof obligaties. Hoewel waterstof bindingen zijn de sterkste van de intermoleculaire krachten, de sterkte van waterstof bindingen is veel minder dan die van ionische bindingen.
Smeltpunt.
| Materiaal | Smeltpunt (°C) |
|---|---|
| ijzer | 1538 |
Aanbevolen:
Hoe kan waterstofbinding tussen watermoleculen helpen bij het verklaren van het vermogen van water om grote hoeveelheden energie te absorberen voordat het verdampt?

Door de waterstofbruggen in water kan het warmte-energie langzamer absorberen en afgeven dan veel andere stoffen. Temperatuur is een maat voor de beweging (kinetische energie) van moleculen. Naarmate de beweging toeneemt, is de energie hoger en dus de temperatuur hoger
Hoe werkt het Aufbau-principe, dat is wat het betekent om te zeggen dat orbitalen van onder naar boven of van boven naar beneden worden gevuld, afhankelijk van het diagram)?

Van beneden naar boven: Kamers moeten vanaf de begane grond worden gevuld. Op hogere verdiepingen kan de volgorde een beetje veranderen. Aufbau-principe: de elektronen vullen de beschikbare orbitalen van de laagste energie tot de hoogste energie. In de grondtoestand bevinden alle elektronen zich in het laagst mogelijke energieniveau
Heeft water een laag smeltpunt?

Water heeft eigenlijk geen laag smeltpunt in vergelijking met andere covalente verbindingen. De meeste covalente verbindingen met een laag molecuulgewicht zijn gasvormig bij kamertemperatuur, terwijl water vloeibaar is. Covalente bindingen zijn sterk genoeg, maar ze zijn beperkt tot individuele moleculen en niet tot het hele stuk van de verbinding
Waarom heeft water een hoog smeltpunt?
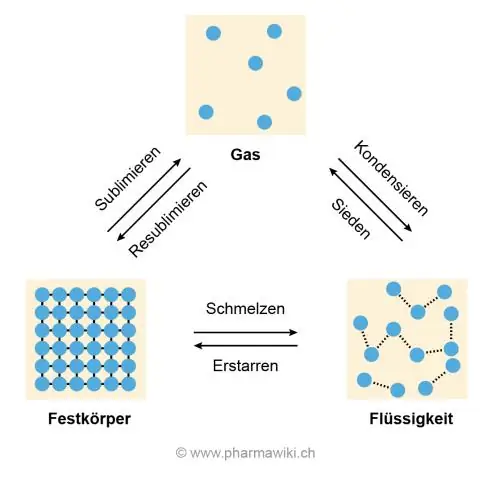
De reden voor de hoge smelt- en kooktemperaturen is de waterstofbinding tussen watermoleculen waardoor ze aan elkaar blijven kleven en niet uit elkaar worden getrokken, wat er gebeurt als ijs smelt en water kookt om een gas te worden
Waarom heeft water een hoog kook- en smeltpunt?

De reden voor de hoge smelt- en kooktemperaturen is de waterstofbinding tussen watermoleculen waardoor ze aan elkaar blijven kleven en niet uit elkaar worden getrokken, wat er gebeurt als ijs smelt en water kookt om een gas te worden
