- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
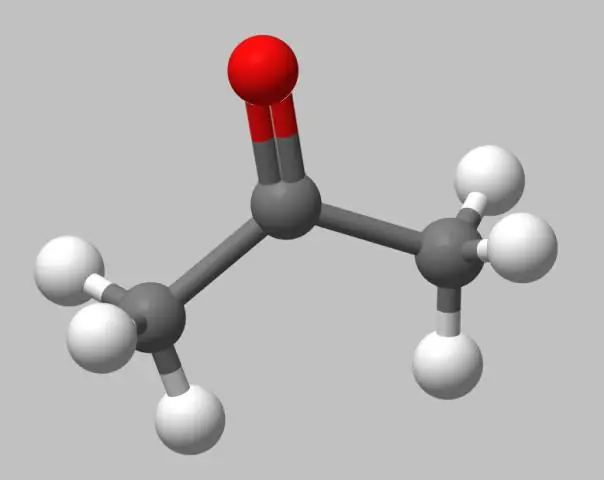
Ball-and-stick-modellen . Ball-and-stick-modellen zijn niet zo realistisch als ruimtevullend modellen , omdat de atomen worden afgebeeld als bollen met stralen die kleiner zijn dan hun van der Waals-stralen. De bindingsregeling is echter gemakkelijker te zien omdat de bindingen expliciet worden weergegeven als: stokjes.
Vervolgens kan men zich ook afvragen, wat stelt het bal- en stickmodel voor?
In de chemie is de bal-en-stok model is een moleculaire model - van een chemische stof die zowel de driedimensionale positie van de atomen als de bindingen daartussen moet weergeven. De atomen zijn meestal vertegenwoordigd door bollen, verbonden door staven die staan voor de obligaties.
En hoe verschilt een ruimtevullend model van een bal- en stokmodel? Bal- en stickmodellen zijn driedimensionaal modellen waar atomen worden weergegeven door bollen van verschillend kleuren en bindingen worden vertegenwoordigd door stokjes tussen de sferen. Ruimtevullende modellen zijn vergelijkbaar met bal en stick modellen in die zin dat ze driedimensionaal zijn modellen die atomen voorstellen als gekleurde bollen.
Hierin, waarom is het bal- en stokmodel niet nauwkeurig?
De bal en stick model is niet een waar weergave van de structuur van kaliumsulfide. 3.3) Zwavel kan ook covalente bindingen vormen. 3.6) Ionische verbindingen zoals kaliumsulfide hebben hoge kookpunten en geleiden elektriciteit wanneer ze in water worden opgelost.
Is water polair of apolair?
Water (H2O) is polair vanwege de gebogen vorm van het molecuul. De vorm betekent dat de meeste negatieve lading van de zuurstof aan de kant van het molecuul en de positieve lading van de waterstofatomen aan de andere kant van het molecuul. Dit is een voorbeeld van polair covalente chemische binding.
Aanbevolen:
Hoe bereken je het gewicht van een bal?

In één oogopslag Om het volume van een bol te bepalen, moet je de diameter nemen tot de macht 3 en deze vermenigvuldigen met Pi en ook met 1/6. Het gewicht van een object wordt berekend door het volume te vermenigvuldigen met de dichtheid van het materiaal
Als een voetballer tegen een bal trapt, versnelt de bal?

Als we de bal trappen, zorgt de kracht die we erop uitoefenen ervoor dat hij versnelt van een snelheid van 0 naar een snelheid van tientallen kilometers per uur. Wanneer de bal van de voet wordt losgelaten, begint deze te vertragen (negatieve versnelling) vanwege de wrijvingskracht die erop wordt uitgeoefend (zoals we in het vorige voorbeeld hebben waargenomen)
Waarom is het een goed idee om alle lagen van je extractie op te slaan tot het einde van het experiment?

Fouten gemaakt tijdens extracties (bijv. doorgaan met de verkeerde laag), kunnen worden opgelost zolang de oplossingen niet in de afvalcontainer zijn geplaatst! De lagen moeten ook worden bewaard tot na verdamping, omdat de gewenste verbinding mogelijk niet erg oplosbaar is in het gebruikte oplosmiddel
Welke golfachtige eigenschap van licht zorgt ervoor dat het van richting verandert wanneer het van het ene medium naar het andere gaat?

breking Wat dit betreft, waarom veranderen golven van richting wanneer ze van het ene materiaal naar het andere reizen? De reden dat de dichtheid het is verander richting is alsof de trillingen verschillende snelheden hebben en door de media gaan.
Strekt een codon zich uit vanaf het ene uiteinde van een tRNA-molecuul?

Het strekt zich uit vanaf het ene uiteinde van een tRNA-molecuul. Het is de basiseenheid van de genetische code. Het bestaat uit drie nucleotiden. Het codeert nooit voor meer dan één aminozuur
