
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
Clausius - Clapeyron-vergelijking - Een voorbeeld.
Bereken de molfractie van water (het oplosmiddel).
- xoplosmiddel = neewater / (Nglucose + neewater).
- Molaire massa van water is 18 G/mol, en voor glucose is het 180,2 G/mol.
- water = 500 / 18 = 27,70 mol.
- glucose = 100 / 180,2 = 0,555 mol.
- xoplosmiddel = 27.70 / (27.70 + 0.555) = 0.98.
Evenzo vragen mensen: wat stelt de Clausius Clapeyron-vergelijking voor?
Meer in het algemeen de Clausius - Clapeyron-vergelijking heeft betrekking op de relatie tussen de druk en temperatuur voor evenwichtsomstandigheden tussen twee fasen. De twee fasen kunnen damp en vast zijn voor sublimatie of vast en vloeibaar om te smelten.
Men kan zich ook afvragen, waar staat C voor in de Clausius Clapeyron-vergelijking? (1) waar ln P is de natuurlijke logaritme van de dampdruk, ∆Hvap is de verdampingswarmte, R is de universele gasconstante (8,31 J·K-1mol-1), T de absolute temperatuur, en C een constante (niet gerelateerd aan warmtecapaciteit).
Ook om te weten, wat is de Clausius Clapeyron-vergelijking en waarom is deze belangrijk?
Clausius - Clapeyron-vergelijking wordt gebruikt voor de volgende doeleinden: Om de dampdruk bij elke temperatuur te schatten. Schatten van de warmteverdamping van faseovergang van de dampdrukken gemeten bij twee temperaturen.
Wat is de vergelijking voor verdampingswarmte?
Gebruik de formule q = m·ΔHv waarin q = warmte energie, m = massa, en ΔHv = warmte van verdamping.
Aanbevolen:
Hoe bereken je de standaarddeviatie van PMP?

De formule die in de PMBOK voor standaarddeviatie wordt gebruikt, is eenvoudig. Het is gewoon (P-O)/6. Dat is de pessimistische schatting van de activiteit minus de optimistische schatting van de activiteit gedeeld door zes. Het probleem is dat deze vorm op geen enkele manier een maat voor standaarddeviatie oplevert
Hoe bereken je de omtrek van de aarde op haar breedtegraad?

De omtrek van een cirkel is gelijk aan 2πr waarbij r de straal is. Op aarde is de omtrek van de bol op een bepaalde breedtegraad 2πr(cos θ) waarbij θ is de breedtegraad en r is de straal van de aarde op de evenaar
Hoe bereken je frequentie uit frequentie en procent?
Om dit te doen, deelt u de frequentie door het totaal aantal resultaten en vermenigvuldigt u met 100. In dit geval is de frequentie van de eerste rij 1 en het totale aantal resultaten is 10. Het percentage zou dan 10,0 zijn. De laatste kolom is Cumulatief percentage
Hoe bereken je potentiële daling in een circuit?
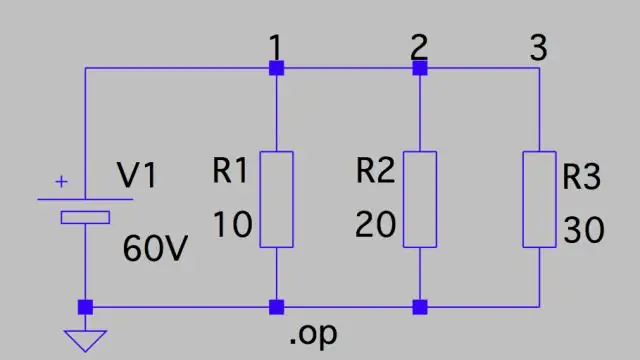
Spanningsval: parallel circuit Dit betekent dat de spanningsval over elk circuit slechts de totale spanning van het circuit is, gedeeld door het aantal weerstanden in het circuit, of 24 V/3 = 8 V
Hoe bereken je hoe ver een object zal reizen?

De afgelegde horizontale afstand kan worden uitgedrukt als x = Vx * t, waarbij t de tijd is. Verticale afstand tot de grond wordt beschreven door de formule y = h + Vy * t – g * t² / 2, waarbij g de zwaartekrachtversnelling is
