
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
Wanneer natrium- en chlooratomen samenkomen om vormen natriumchloride ( NaCl ), zij overdracht een elektron . Met de overdracht van de elektron ze worden echter elektrisch geladen en combineren tot zouten via de vorming van ionbindingen. Het natriumion heeft nu nog maar tien elektronen , maar heeft nog steeds elf protonen.
In dit opzicht, hoe wordt natriumchloride gevormd door overdracht van elektronen. Waarom geleidt de oplossing van natriumchloride elektriciteit?
Natriumchloride is een ionische verbinding die bestaat uit Natrium ion en Chloride ion. in vast formulier band tussen deze twee is erg sterk. Maar in water worden de ionen vrij en bewegen ze willekeurig. Deze ionen zijn ladingsdragers en dus verantwoordelijk voor: elektriciteit geleiding.
En welk effect heeft de overdracht van elektronen op de kern? elektronen zijn de negatief geladen deeltjes van een atoom. Samen, alle elektronen van een atoom een negatieve lading creëren die de positieve lading van de protonen in het atoom in evenwicht houdt kern . elektronen zijn extreem klein in vergelijking met alle andere delen van het atoom.
Met dit in het achterhoofd, wat voor soort binding is het resultaat van de overdracht van een elektron?
De vorming van een Ionische obligatie is het resultaat van de overdracht van een of meer elektronen van een metaal naar een niet-metaal. Covalent Bonding : Bonding tussen niet-metalen bestaat uit twee elektronen gedeeld tussen twee atomen. in covalent binding , de twee elektronen die door de atomen worden gedeeld, worden aangetrokken door de kern van beide atomen.
Is natriumchloride een goede geleider van elektriciteit?
In de vaste toestand, ionische verbindingen zoals natriumchloride hebben hun ionen op hun plaats gefixeerd en daarom kunnen deze ionen niet bewegen, dus vaste ionische verbindingen kunnen niet geleiden elektriciteit . In gesmolten toestand zijn ionen in ionische verbindingen echter vrij om te stromen en daarom gesmolten natriumchloride kan leiden elektriciteit.
Aanbevolen:
Wat is de naam van het zout dat wordt gevormd door de neutralisatie van zoutzuur en natriumhydroxide?
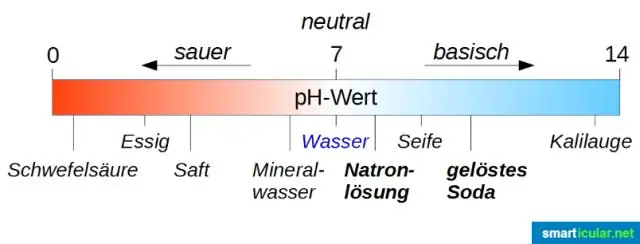
Toelichting: De reactie tussen natriumhydroxide (NaOH) en zoutzuur (HCl) is een neutralisatiereactie die resulteert in de vorming van een zout, natriumchloride (NaCl) en water (H2O). Het is een exotherme reactie
Welk type halfgeleider wordt gevormd wanneer germanium wordt gedoteerd met aluminium?

P-type halfgeleider wordt gevormd wanneer Ge(gp-14) wordt gedoteerd met Al(gp-13). Er wordt één elektronengat gecreëerd
Wat is het organische product dat wordt gevormd door de dehydratatie van 3 Methyl 2 Pentanol?

Door zuur gekatalyseerde dehydratatie van 3-methyl-2-pentanol geeft drie alkenen: 3-methyl-1-penteen, 3-methyl-2-penteen en 3-methyleenpentaan. Teken de structuur van het carbokation-tussenproduct dat leidt tot de vorming van 3-methyl-2-penteen
Hoe wordt het pad van de fotonen door het plasma van de zon genoemd?

De stralingszone is de tweede laag (van binnenuit naar buiten) van de zon. De energie beweegt langzaam naar buiten. het pad van fotonen door het plasma van de zon
Hoe wordt mechanische energie behouden tijdens overdracht of transformatie?

De wet van behoud van energie stelt dat voor elk systeem energie niet kan worden gecreëerd of vernietigd; het kan alleen van de ene vorm naar de andere veranderen of van het ene object naar het andere overgaan. Mechanische energie is er in twee vormen: potentiële energie, wat opgeslagen energie is, en kinetische energie, wat bewegingsenergie is
