
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
EEN wrat is een chemisch teleenheid, zodanig dat 1 wrat = 6.022*1023 deeltjes. Stoichiometrie vereist ook het gebruik van evenwichtige vergelijkingen . Van de evenwichtige vergelijking we kunnen de molverhouding . De molverhouding is de verhouding van mollen van een stof aan de mollen van een andere stof in a evenwichtige vergelijking.
Precies, hoeveel mol zit er in 1 kg NaCl?
De SI-basiseenheid voor de hoeveelheid stof is de mol. 1 mol is gelijk aan 1 mol NaCl, of 58.44277 gram.
Evenzo, hoe bepaal je de stoichiometrische verhouding? Dus, om de te berekenen stoïchiometrie in massa wordt het aantal moleculen dat nodig is voor elke reactant uitgedrukt in mol en vermenigvuldigd met de molaire massa van elk om de massa van elke reactant per mol reactie te geven. De massa verhoudingen kan worden berekend door elk te delen door het totaal in de hele reactie.
Weet ook, wat is de molverhouding?
de verhouding tussen de bedragen in mollen van twee verbindingen die betrokken zijn bij een chemische reactie. molverhoudingen worden gebruikt als conversiefactoren tussen producten en reactanten in veel chemieproblemen.
Waarom is de molverhouding belangrijk?
1 Antwoord. molverhoudingen zijn belangrijk omdat molverhoudingen sta je toe om te veranderen mollen van een stof om mollen van een andere stof. De molverhouding is de magie die verandert van A naar B. The molverhoudingen komen van de chemische formule of vergelijking.
Aanbevolen:
Hoe vind je de vergelijking van een lijn loodrecht op één punt?
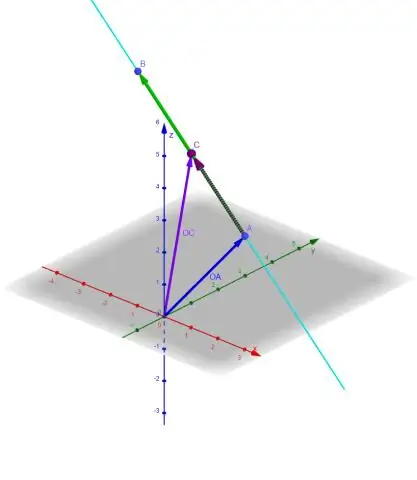
Zet eerst de vergelijking van de gegeven lijn in de vorm van helling-snijpunt door op te lossen voor y. Je krijgt y = 2x +5, dus de helling is –2. Loodrechte lijnen hebben tegengestelde-reciproke hellingen, dus de helling van de lijn die we willen vinden is 1/2. Als we het gegeven punt in de vergelijking y = 1/2x + b invoeren en oplossen voor b, krijgen we b = 6
Hoe weet je of een nieuwe stof wordt gevormd in een chemische vergelijking?

Er zijn tekenen dat er een chemische reactie optreedt. Er vormen zich bellen, er komt een gas vrij en de beker wordt erg heet. Het belangrijkste teken dat er een chemische reactie plaatsvindt, is de vorming van nieuwe stoffen. De nieuwe stoffen zijn koolstof, een brosse zwarte vaste stof, en waterdamp, een kleurloos gas
Hoe vind je de vergelijking van een lijn gegeven een punt en een parallelle lijn?
De vergelijking van de lijn in de vorm van het helling-snijpunt is y=2x+5. De helling van de parallellijn is hetzelfde: m=2. De vergelijking van de parallelle lijn is dus y=2x+a. Om a te vinden, gebruiken we het feit dat de lijn door het gegeven punt moet gaan:5=(2)⋅(&min;3)+a
Hoe vind je het domein van een beperking in een vergelijking?

How To: Gegeven een functie geschreven in een vergelijkingsvorm die een breuk bevat, zoek het domein. Identificeer de invoerwaarden. Identificeer eventuele beperkingen op de invoer. Als er een noemer in de formule van de functie staat, stel de noemer dan gelijk aan nul en los op voor x
Wat is een voorbeeld van een skelet-chemische vergelijking?

Voorbeelden: Als we doorgaan met de elektrolyse van water, hebben we een skeletvergelijking, '' De formule voor water is H2O; de formule voor waterstof is H2; en de formule voor zuurstof is O2. Een skeletvergelijking is slechts een manier om de formules te gebruiken om de chemicaliën aan te geven die bij de chemische reactie betrokken waren
