
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
E1 geeft a. aan eliminatie , unimoleculaire reactie , waar tarief = k [R-LG]. in een E1 reactie , de tarief bepalende stap is het verlies van de vertrekkende groep om het intermediaire carbokation te vormen. Hoe stabieler het carbokation is, hoe gemakkelijker het is om te vormen en hoe sneller de E1 reactie zal zijn.
Zo ja, hoe doe je een e1-reactie?
Een E1 reactie omvat de deprotonering van een waterstof in de buurt (meestal één koolstof verwijderd, of de bèta-positie) de carbokation resulterend in de vorming van een alkeenproduct. Om dit te bereiken, is een Lewis-base vereist.
Wat is ook het verschil tussen de e1- en e2-reactie? mechanisch, E2 reacties zijn gecoördineerd (en komen sneller voor), terwijl E1 reacties zijn stapsgewijs (en treden over het algemeen langzamer en tegen hogere energiekosten op). Vanwege E1's mechanisch gedrag kunnen herschikkingen van carbocatie optreden in de intermediair, zodat de positieve lading wordt verplaatst naar de meest stabiele koolstof.
Als je dit in overweging neemt, wat is dan de snelheidsvergelijking van een e2-reactie?
E2 geeft een aan eliminatie , bimoleculaire reactie , waar tarief = k [B][R-LG]. in een E2 reactie , de reactie transformeert 2 sp3 C-atomen in sp2 C atomen. Dit verplaatst de substituenten verder uit elkaar, waardoor sterische interacties worden verminderd. Dus meer sterk gesubstitueerde systemen ondergaan E2 eliminaties sneller.
Is een e1-reactie gecoördineerd?
Dus hoe stabieler de carbokation is, hoe sneller de reactie zal zijn. De koers van de E2 reactie hangt af van zowel substraat als base, aangezien de snelheidsbepalende stap bimoleculair is ( overlegd ). Over het algemeen is een sterke base vereist, een die verplaatsing van een polaire vertrekkende groep mogelijk maakt.
Aanbevolen:
Wat is de eerste stap bij het construeren van een loodlijn van een punt op een lijn?
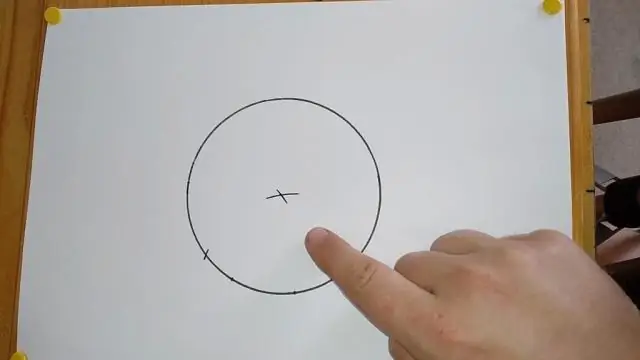
Verbind het gegeven punt met het punt waar de bogen elkaar kruisen. Gebruik een liniaal om ervoor te zorgen dat de lijn recht is. De lijn die je tekent staat loodrecht op de eerste lijn, door het gegeven punt op de lijn
Hoe schrijf je een breuk als een product van een geheel getal en een eenheidsbreuk?

Regels om het product van een eenheidsbreuk en een geheel getal te vinden We schrijven het gehele getal eerst als een breuk, d.w.z. door het te delen door één; bijvoorbeeld: 7 wordt geschreven als 71. We vermenigvuldigen dan de tellers. We vermenigvuldigen de noemers. Als er een vereenvoudiging nodig is, is het klaar en dan schrijven we de laatste breuk
Wat is een voorbeeld van een gedeelde afgeleide eigenschap van een primaat?

Apomorfie - een afgeleide eigenschap die niet wordt gevonden in de voorouder, maar wel aanwezig is in afstammelingen, bijvoorbeeld nagels bij primaten. Autapomorphy - een unieke afgeleide eigenschap die aanwezig is in lidsoorten van een bepaalde graad, bijvoorbeeld het ontbreken van een staart bij apen
Wat is de flux door een kubus van zijde als een puntlading van Q zich in een van zijn hoeken bevindt?

Zoals we dat weten, is de totale flux van een lading q q/ε0 (wet van Gauss). Als de lading zich op de hoek van een kubus bevindt, komt een deel van de flux de kubus binnen en verlaat deze via enkele van zijn vlakken. Maar een deel van de flux komt niet in de kubus. Deze 1/8e wordt weer opgedeeld in 3 delen
Wat zijn de voordelen van het gebruik van een oven in plaats van een vlam bij atomaire absorptie?

Noem de voor- en nadelen van een oven in vergelijking met het gebruik van een vlam bij atoomabsorptiespectroscopie. De belangrijkste voordelen zijn een grotere gevoeligheid (concentratie en vooral massa). De belangrijkste nadelen zijn een grotere instrumentcomplexiteit en instrumentkosten
