
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
EEN molverhouding is een omrekeningsfactor die de bedragen in mollen van twee stoffen in een chemische reactie. De getallen in een conversiefactor zijn afkomstig van de coëfficiënten van de uitgebalanceerde chemische vergelijking. De volgende zes molverhoudingen kan worden geschreven voor de ammoniakvormende reactie hierboven.
Daarvan, hoe vind je de molverhouding?
- Begin met het aantal grammen van elk element, gegeven in de opgave.
- Converteer de massa van elk element naar mol met behulp van de molaire massa uit het periodiek systeem.
- Deel elke molwaarde door het kleinste aantal berekende mollen.
- Rond af op het dichtstbijzijnde gehele getal. Dit is de molverhouding van de elementen en is.
Bovendien, waarom is de molverhouding belangrijk? molverhoudingen zijn belangrijk omdat molverhoudingen sta je toe om te veranderen mollen van een stof om mollen van een andere stof. De molverhouding is de magie die verandert van A naar B. The molverhoudingen komen van de chemische formule of vergelijking.
wat is een molverhouding?
de verhouding tussen de bedragen in mollen van twee verbindingen die betrokken zijn bij een chemische reactie. molverhoudingen worden gebruikt als conversiefactoren tussen producten en reactanten in veel chemieproblemen.
Wat is molconversie?
Converteren van mollen naar volume (liters): Vermenigvuldig uw wrat waarde door de molaire volumeconstante, 22.4L. Converteren van deeltjes (atomen, moleculen of formule-eenheden) naar mollen : Deel uw deeltjeswaarde door het getal van Avogadro, 6.02×1023.
Aanbevolen:
Hoe schrijf je de formule voor een verbinding die een polyatomisch ion bevat?
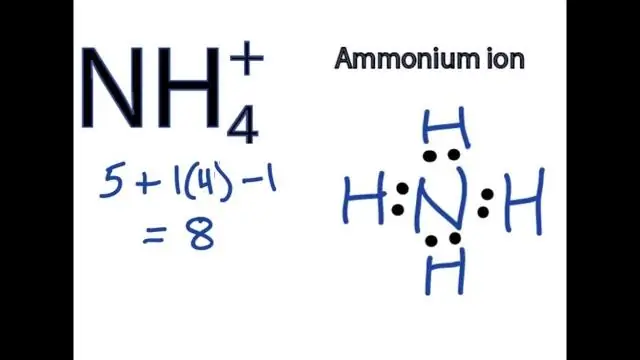
Om formules te schrijven voor verbindingen die polyatomaire ionen bevatten, schrijft u het symbool voor het metaalion gevolgd door de formule voor het polyatomaire ion en brengt u de ladingen in evenwicht. Om een verbinding te noemen die een polyatomisch ion bevat, vermeldt u eerst het kation en vervolgens het anion
Hoe vind je de molverhouding in een chemische vergelijking?

Een mol is een chemische teleenheid, zodanig dat 1 mol = 6.022*1023 deeltjes. Stoichiometrie vereist ook het gebruik van gebalanceerde vergelijkingen. Uit de gebalanceerde vergelijking kunnen we de molverhouding krijgen. De molverhouding is de verhouding van het aantal mol van de ene stof tot het aantal mol van een andere stof in een evenwichtige vergelijking
Hoe schrijf je een breuk als een product van een geheel getal en een eenheidsbreuk?

Regels om het product van een eenheidsbreuk en een geheel getal te vinden We schrijven het gehele getal eerst als een breuk, d.w.z. door het te delen door één; bijvoorbeeld: 7 wordt geschreven als 71. We vermenigvuldigen dan de tellers. We vermenigvuldigen de noemers. Als er een vereenvoudiging nodig is, is het klaar en dan schrijven we de laatste breuk
Wat is een molverhouding en hoe wordt deze gebruikt in stoichiometrie?

Molaire verhoudingen worden gebruikt als vergelijkingsmiddel voor stoffen in een uitgebalanceerde chemische vergelijking om hoeveelheden te bepalen. Hoeveel mol waterstofgas zijn er nodig om te reageren met 5 mol stikstof. We kunnen conversiefactoren gebruiken in een proces dat stoichiometrie wordt genoemd. Molverhouding biedt een vergelijking om eenheden te annuleren
Hoe schrijf je een vergelijking in de vorm van een hellingsintercept voor een tabel?
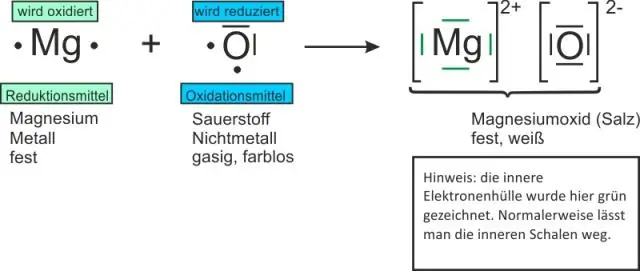
Neem de vergelijking y = mx + b en vul de m-waarde (m = 1) en een paar (x, y) coördinaten uit de tabel in, zoals (5, 3). Los dan op voor b. Gebruik ten slotte de gevonden m- en b-waarden (m = 1 en b = -2) om de vergelijking te schrijven
