
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
orbitalen definieer gebieden in de ruimte waar je waarschijnlijk elektronen zult vinden. s orbitalen (ℓ = 0) zijn bolvormig gevormd . p orbitalen (ℓ = 1) zijn halters gevormd . De drie mogelijke p orbitalen staan altijd loodrecht op elkaar.
Weet ook, wat is de vorm van de P-orbitaal?
EEN p orbitaal heeft de geschatte vorm van een paar lobben aan weerszijden van de kern, of een enigszins halter vorm . Een elektron in a p orbitaal gelijke kans heeft om in een van beide helften te zitten.
Evenzo, wat zijn de vormen van SP- en d-orbitalen? De dXY, dYZ en dZX orbitalen heb hetzelfde vorm d.w.z. klaverblad vorm maar ze liggen respectievelijk in XY-, YZ- en ZX-vlakken. Het dZ-vierkant orbitaal is symmetrisch om de Z-as en heeft een stomme bel vorm met een donutvorm elektron wolk in het midden.
Trouwens, wat is de vorm van S en P Subshell?
Zowel de 1n als de 2n hoofdschil hebben een s orbitaal, maar de grootte van de bol is groter in de 2n orbitaal. Elke bol is een enkele orbitaal. p subshells bestaan uit drie halter- gevormde orbitalen . Hoofdschil 2n heeft een p subshell , maar shell 1 niet.
Wat zijn de kenmerken van een s-orbitaal?
De s-orbitaal is een bolvormig gebied dat beschrijft waar een elektron kan worden gevonden, binnen een bepaalde mate van waarschijnlijkheid. De vorm van de orbitaal hangt af van de kwantumgetallen die bij een energietoestand horen. Alle s-orbitalen hebben l = m = 0, maar de waarde van n kan variëren.
Aanbevolen:
Wat is de vorm van het pad dat elke planeet volgt terwijl deze om de zon draait?

Planeten draaien om de zon in ovaalvormige paden die ellipsen worden genoemd, met de zon iets uit het midden van elke ellips. NASA heeft een vloot ruimtevaartuigen die de zon observeren om meer te weten te komen over de samenstelling ervan en om betere voorspellingen te doen over zonneactiviteit en het effect ervan op aarde
Hoe verschilt de vorm van een plantencel van die van een dierlijke cel?
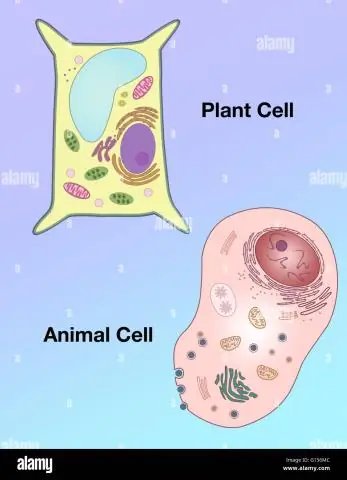
Vacuolen: Plantencellen hebben een grote vacuole, terwijl dierlijke cellen meerdere kleine vacuolen bevatten. Vorm: Plantencellen hebben een meer regelmatige vorm (meestal rechthoekig), terwijl dierlijke cellen onregelmatige vormen hebben. Lysosomen: zijn over het algemeen aanwezig in dierlijke cellen, terwijl ze afwezig zijn in plantencellen
Wat is de derdemachtswortel van 40 in radicale vorm?

De factor 40 waarvan we de derdemachtswortel kunnen nemen is 8. We kunnen 40 schrijven als (8)(5) en dan de productregel van radicalen gebruiken om de 2 getallen te scheiden. We kunnen de derdemachtswortel van 8 nemen, wat 2 is, maar we zullen de 5 onder de derdemachtswortel moeten laten
Welke fase van materie neemt de vorm aan van zijn container?

Vloeistof Met dit in het achterhoofd, welke substantie neemt niet de vorm aan van zijn container? vast: A substantie dat behoudt zijn maat en vorm zonder een container ; een substantie waarvan de moleculen niet vrij kunnen bewegen, behalve om te trillen.
Waarom heeft het veranderen van de vorm geen effect op de dichtheid van het object?

Het veranderen van de vorm van een object zal de dichtheid van een object niet veranderen omdat de massa en het volume hetzelfde blijven. Dus dan blijft de dichtheid hetzelfde. Een luchtbel stijgt naar het oppervlak van een glas water w=1 g/ml omdat de luchtbel een lagere dichtheid heeft dan het water
