
Inhoudsopgave:
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
Titratieprobleem Stapsgewijze oplossing
- Stap 1: Bepaal [OH-] Elke mol NaOH heeft één mol OH-.
- Stap 2: Bepaal het aantal mol OH- Molariteit = aantal mol/volume.
- Stap 3: Bepaal het aantal mol H+
- Stap 4: Bepaal de concentratie HCl.
Op dezelfde manier kan men zich afvragen, hoe bereken je titratie?
Gebruik de titratie formule. Als de titrant en analyt een molverhouding van 1:1 hebben, is de formule molariteit (M) van het zuur x volume (V) van het zuur = molariteit (M) van de base x volume (V) van de base. (Molariteit is de concentratie van een oplossing uitgedrukt als het aantal mol opgeloste stof per liter oplossing.)
Wat is naast bovenstaande de molariteit van NaOH? Bijvoorbeeld een 0,25 M NaOH oplossing (dit wordt gelezen als 0,25 molair) bevat 0,25 mol natriumhydroxide in elke liter oplossing. Elke keer dat je de afkorting M ziet, moet je het meteen zien als mol/L.
Hiervan, hoe vind je de concentratie HCl uit titratie met NaOH?
Bereken de concentratie van het zoutzuur
- Volume natriumhydroxideoplossing = 25,00 ÷ 1000 = 0,0250 dm 3
- Hoeveelheid natriumhydroxide = 0,200 x 0,0250 = 0,005 mol.
- Uit de vergelijking reageert 0,005 mol NaOH met 0,005 mol HCl.
- Volume zoutzuur = 22,70 ÷ 1000 = 0,0227 dm 3
Wat is indicator bij titratie?
Indicator : Een stof die van kleur verandert als reactie op een chemische verandering. Een zuur-base indicator (bijv. fenolftaleïne) verandert van kleur afhankelijk van de pH. Redox indicatoren worden ook gebruikt. Een druppel van indicator oplossing wordt toegevoegd aan de titratie in het begin; het eindpunt is bereikt wanneer de kleur verandert.
Aanbevolen:
Hoe bereken je de standaarddeviatie van PMP?

De formule die in de PMBOK voor standaarddeviatie wordt gebruikt, is eenvoudig. Het is gewoon (P-O)/6. Dat is de pessimistische schatting van de activiteit minus de optimistische schatting van de activiteit gedeeld door zes. Het probleem is dat deze vorm op geen enkele manier een maat voor standaarddeviatie oplevert
Hoe bereken je de omtrek van de aarde op haar breedtegraad?

De omtrek van een cirkel is gelijk aan 2πr waarbij r de straal is. Op aarde is de omtrek van de bol op een bepaalde breedtegraad 2πr(cos θ) waarbij θ is de breedtegraad en r is de straal van de aarde op de evenaar
Hoe bereken je frequentie uit frequentie en procent?
Om dit te doen, deelt u de frequentie door het totaal aantal resultaten en vermenigvuldigt u met 100. In dit geval is de frequentie van de eerste rij 1 en het totale aantal resultaten is 10. Het percentage zou dan 10,0 zijn. De laatste kolom is Cumulatief percentage
Hoe bereken je potentiële daling in een circuit?
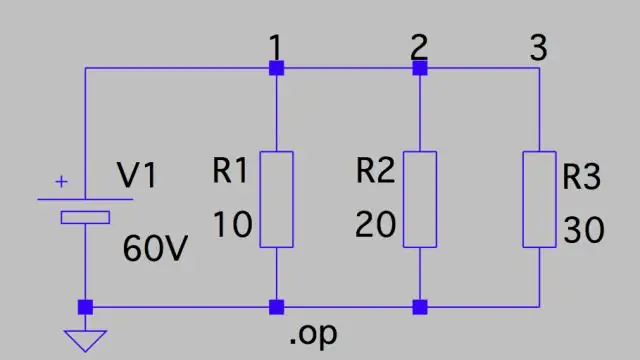
Spanningsval: parallel circuit Dit betekent dat de spanningsval over elk circuit slechts de totale spanning van het circuit is, gedeeld door het aantal weerstanden in het circuit, of 24 V/3 = 8 V
Hoe bereken je hoe ver een object zal reizen?

De afgelegde horizontale afstand kan worden uitgedrukt als x = Vx * t, waarbij t de tijd is. Verticale afstand tot de grond wordt beschreven door de formule y = h + Vy * t – g * t² / 2, waarbij g de zwaartekrachtversnelling is
