
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
Reactie tussenproducten worden in één gevormd stap en vervolgens geconsumeerd in een later stap van de reactiemechanisme: . De langzaamste stap in de mechanisme heet de koersbepalend of snelheidsbeperkend stap . de algemene reactie tarief wordt bepaald door de tarieven van de stappen tot (en met) de snelheidsbepalende stap.
Ook om te weten is, hoe vind je de langzaamste stap in een reactie?
De beoordeling bepalende stap is de langzaamste stap van een chemische stof reactie dat bepaalt de snelheid (snelheid) waarmee de algehele reactie opbrengst.
Antwoord geven
- De snelheidsbepalende stap is de tweede stap omdat het de langzame stap is.
- 2NO+2H2→N2+2H2O.
- De tussenproducten in deze reactie zijn N2O2 en N2O.
Bovendien, wat is een eerste-ordereactie? EEN eerst - bestelling reactie is een reactie dat verloopt met een snelheid die lineair afhangt van slechts één reactantconcentratie.
Ook om te weten is, waarom de snelheidsbepalende stap de langzaamste stap is in een reactiemechanisme?
De tarief - bepalende stap is de langzaamste stap in een reactiemechanisme . Omdat het de langzaamste , het bepaalt de tarief van de overall reactie . Dit zal later in meer detail worden onderzocht. Verandering in concentratie van chemicaliën in de tijd: een grafiek van tijd versus concentratie voor twee soorten in chemisch evenwicht.
Hoe vind je de algemene reactie?
De algemene reactie snelheid wordt bepaald door de snelheden van de stappen tot (en inclusief) de langzaamste elementaire stap. De langzaamste stap in a reactie mechanisme wordt de snelheidsbepalende of snelheidsbeperkende stap genoemd. Voor ons voorbeeldmechanisme in de vorige sectie is de snelheidsbeperkende stap de eerste elementaire stap.
Aanbevolen:
Welk effect heeft een katalysator op het mechanisme van een reactie?

Een katalysator versnelt een chemische reactie, zonder door de reactie te worden verbruikt. Het verhoogt de reactiesnelheid door de activeringsenergie voor een reactie te verlagen
Wat is de eerste stap bij het construeren van een loodlijn van een punt op een lijn?
Verbind het gegeven punt met het punt waar de bogen elkaar kruisen. Gebruik een liniaal om ervoor te zorgen dat de lijn recht is. De lijn die je tekent staat loodrecht op de eerste lijn, door het gegeven punt op de lijn
Hoe doe je de elektronenconfiguratie stap voor stap?

Stappen Zoek het atoomnummer van uw atoom. Bepaal de lading van het atoom. Onthoud de basislijst van orbitalen. Begrijp de notatie van de elektronenconfiguratie. Onthoud de volgorde van de orbitalen. Vul de orbitalen in volgens het aantal elektronen in je atoom. Gebruik het periodiek systeem als een visuele snelkoppeling
Hoe teken je een vergelijking stap voor stap?
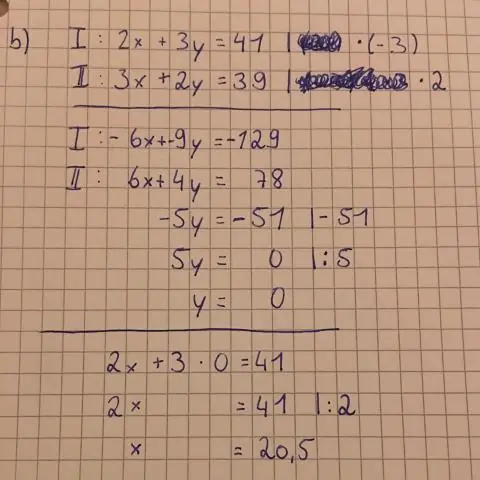
Hier zijn enkele te volgen stappen: Vul x = 0 in de vergelijking in en los op voor y. Zet het punt (0,y) op de y-as. Vul y = 0 in de vergelijking in en los op voor x. Teken het punt (x,0) op de x-as. Trek een rechte lijn tussen de twee punten
Hoe maak je stap voor stap een helling?

Er zijn drie stappen bij het berekenen van de helling van een rechte lijn als u de vergelijking niet krijgt. Stap één: identificeer twee punten op de lijn. Stap twee: Selecteer een om (x1, y1) te zijn en de andere om (x2, y2) te zijn. Stap drie: gebruik de hellingsvergelijking om de helling te berekenen
