
Inhoudsopgave:
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-06-01 05:05.
De pH van zoutoplossingen berekenen
- massa NaF = 20,0 g.
- molmassa NaF = 41,99 g/mol.
- volume oplossing = 0,500 L.
- uit - = 1.4 × 10 −11
Evenzo, hoe vind je de pH van een zoutoplossing?
geconjugeerd zuur-basepaar. Zouten kan zuur, neutraal of basisch zijn. Zouten die gevormd worden uit een sterk zuur en een zwakke base zijn zuur zouten , zoals ammoniumchloride (NH4Cl).
En wat is de pH van Na? pH van gewone zuren en basen
| Baseren | Naam | 1 mM |
|---|---|---|
| Sr(OH)2 | strontiumhydroxide | 11.27 |
| NaOH | natriumhydroxide | 10.98 |
| KOH | kaliumhydroxide (kaliloog) | 10.98 |
| Na2SiO3 | natriummetasilicaat | 11.00 |
Evenzo, hoe vind je de pH van een oplossing?
Tot bereken de pH van een waterige oplossing jij moet ken de concentratie van het hydroniumion in mol per liter (molariteit). De pH wordt dan berekend met behulp van de uitdrukking: pH = - log [H3O+].
Wat is de pH van zout water?
de geaccepteerde pH niveau in een basis zout water systeem ligt tussen 7,6 en 8,4, maar riftanks zijn gevoeliger en moeten daarom aan de bovenkant van de pH schaal, 8,0 tot 8,4.
Aanbevolen:
Hoe verschilt de vorm van een plantencel van die van een dierlijke cel?
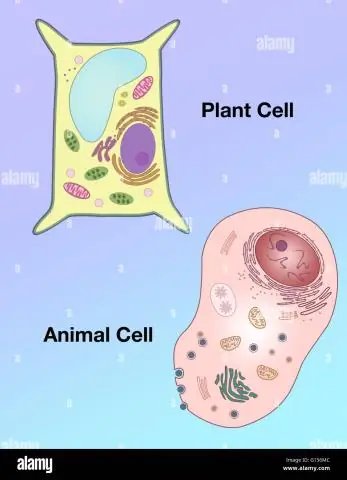
Vacuolen: Plantencellen hebben een grote vacuole, terwijl dierlijke cellen meerdere kleine vacuolen bevatten. Vorm: Plantencellen hebben een meer regelmatige vorm (meestal rechthoekig), terwijl dierlijke cellen onregelmatige vormen hebben. Lysosomen: zijn over het algemeen aanwezig in dierlijke cellen, terwijl ze afwezig zijn in plantencellen
Hoe bereken je de resulterende kracht met behulp van een parallellogram van krachten?

Om de resultante te vinden, zou je een parallellogram maken met de zijden gelijk aan de twee uitgeoefende krachten. De diagonaal van dit parallellogram is dan gelijk aan de resulterende kracht. Dit wordt het krachtenparallellogram genoemd
Hoe schrijf je een breuk als een product van een geheel getal en een eenheidsbreuk?

Regels om het product van een eenheidsbreuk en een geheel getal te vinden We schrijven het gehele getal eerst als een breuk, d.w.z. door het te delen door één; bijvoorbeeld: 7 wordt geschreven als 71. We vermenigvuldigen dan de tellers. We vermenigvuldigen de noemers. Als er een vereenvoudiging nodig is, is het klaar en dan schrijven we de laatste breuk
Hoe bereken je de kans dat een gebeurtenis minstens één keer voorkomt?

Om de kans te berekenen dat een gebeurtenis minstens één keer voorkomt, is dit het complement van de gebeurtenis die nooit voorkomt. Dit betekent dat de kans dat de gebeurtenis nooit optreedt en de kans dat de gebeurtenis zich minstens één keer voordoet gelijk is aan één of 100% kans
Wat is de flux door een kubus van zijde als een puntlading van Q zich in een van zijn hoeken bevindt?

Zoals we dat weten, is de totale flux van een lading q q/ε0 (wet van Gauss). Als de lading zich op de hoek van een kubus bevindt, komt een deel van de flux de kubus binnen en verlaat deze via enkele van zijn vlakken. Maar een deel van de flux komt niet in de kubus. Deze 1/8e wordt weer opgedeeld in 3 delen
