
- Auteur Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Laatst gewijzigd 2025-01-22 17:06.
De waterstof heeft dan de gedeeltelijke positieve lading. Om de mogelijkheid te herkennen van waterstofbinding , onderzoek de Lewis-structuur van de molecuul . Het elektronegatieve atoom moet een of meer ongedeelde elektronenparen hebben zoals in het geval van zuurstof en stikstof, en heeft een negatieve gedeeltelijke lading.
Daarnaast, welk molecuul heeft waterstofbinding?
water
Bovendien, is water polair of niet-polair? Water (H2O) is polair vanwege de gebogen vorm van het molecuul. De vorm betekent dat de meeste negatieve lading van de zuurstof aan de kant van het molecuul en de positieve lading van de waterstofatomen aan de andere kant van het molecuul. Dit is een voorbeeld van polair covalente chemische binding.
Ten tweede, hoe wordt de sterkte van waterstofbruggen bepaald?
1 waterstofbinding . Waterstofbruggen worden gevormd tussen een elektronegatief atoom en a waterstof atoom gebonden aan een tweede elektronegatief atoom [80]. De kracht van de waterstofbinding hangt af van de elektronegativiteit van de atomen; Tabel 1 classificeert waterstofbruggen als zeer sterk (bijv. [F…H… F]−), sterk (bijv. O H …
Waarom zijn waterstofbruggen belangrijk?
waterstofbinding is belangrijk in veel chemische processen. waterstofbinding is verantwoordelijk voor de unieke oplosmiddelcapaciteiten van water. Waterstofbruggen houden complementaire DNA-strengen bij elkaar en ze zijn verantwoordelijk voor het bepalen van de driedimensionale structuur van gevouwen eiwitten, inclusief enzymen en antilichamen.
Aanbevolen:
Kan een niet-polair molecuul waterstofbruggen hebben?

Als het molecuul niet-polair is, kunnen er geen dipool-dipool-interacties of waterstofbindingen optreden en is de enige mogelijke intermoleculaire kracht de zwakke van der Waals-kracht
Waarom is het bal- en stokmodel van een molecuul een onrealistisch beeld?
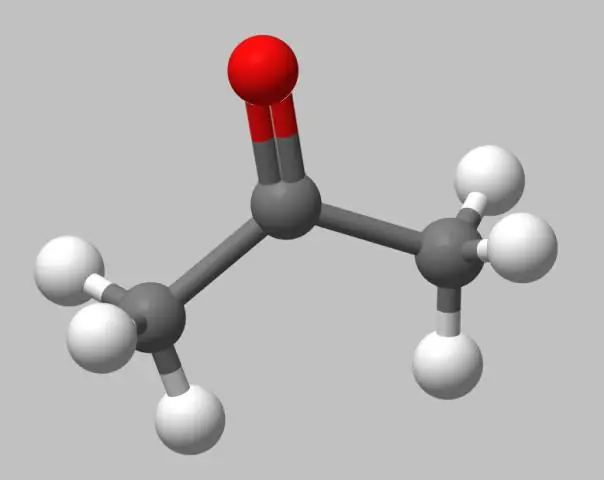
Ball-and-stick modellen. Ball-and-stick-modellen zijn niet zo realistisch als ruimtevullende modellen, omdat de atomen worden afgebeeld als bollen met stralen die kleiner zijn dan hun van der Waals-stralen. De bindingsregeling is echter gemakkelijker te zien omdat de bindingen expliciet worden weergegeven als sticks
Kan een molecuul chiraal zijn zonder een stereocentrum?

Chirale verbindingen zonder stereocentra [bewerken] Het is ook mogelijk dat een molecuul bechiraal is zonder werkelijke puntchiraliteit (stereocentra). Veel voorkomende voorbeelden zijn 1,1'-bi-2-naftol (BINOL) en 1,3-dichloor-alleen die axiale chiraliteit hebben, en (E)-cycloocteen die planarchiraliteit heeft
Hoe weet je of een transformatie één op één is?
Wanneer een lineaire transformatie wordt beschreven in termen van een matrix, is het gemakkelijk om te bepalen of de lineaire transformatie één-op-één is of niet door de lineaire afhankelijkheid van de kolommen van de matrix te controleren. Als de kolommen lineair onafhankelijk zijn, is de lineaire transformatie één-op-één
Hoe kan een geoloog zien of een vouw een syncline en een anticlinaal is?

Geologische structuren (Deel 5) Anticlinen zijn plooien waarin elke helft van de plooi wegvalt van de top. Synclines zijn plooien waarbij elke helft van de vouw naar het dal van de vouw zakt. U kunt het verschil onthouden door op te merken dat anticlines een "A" -vorm vormen en synclines de onderkant van een "S"
